দশম শ্ৰেণী বিজ্ঞান অধ্যায় ১ – ৰাসায়নিক বিক্ৰিয়া আৰু সমীকৰণ – সম্পূৰ্ণ পাঠ্যভিত্তিক প্ৰশ্নোত্তৰ | ASSEB Assam (Assamese Medium)
দশম শ্ৰেণী বিজ্ঞান অধ্যায় ১ – ৰাসায়নিক বিক্ৰিয়া আৰু সমীকৰণ সম্পূৰ্ণ পাঠ্যভিত্তিক প্ৰশ্নোত্তৰ আৰু সমাধান (ASSEB / SEBA Assam – Assamese Medium)
দশম শ্ৰেণীৰ বিজ্ঞান (Science) পাঠ্যক্ৰমৰ প্ৰথম অধ্যায় ‘ৰাসায়নিক বিক্ৰিয়া আৰু সমীকৰণ’ (Chemical Reactions and Equations) এখন অতি গুৰুত্বপূৰ্ণ পাঠ। আগন্তুক মেট্ৰিক পৰীক্ষাৰ বাবে নতুন ASSEB (Assam State School Education Board) পাঠ্যক্ৰম আৰু নৱ্য শিক্ষা নীতিৰ (NEP) শেহতীয়া নিৰ্দেশনাৰ আধাৰত এই অধ্যায়ৰ সম্পূৰ্ণ পাঠ্যভিত্তিক প্ৰশ্নোত্তৰ (Class 10 Science Chapter 1 Textual Question Answer) প্ৰস্তুত কৰা হৈছে। এই বিশেষ সংকলনটিত পাঠভিত্তিক অতি চমু প্ৰশ্ন (VSA), চমু প্ৰশ্ন (Short Questions), দীঘলীয়া প্ৰশ্ন (Long Answers), আৰু ৰাসায়নিক সমীকৰণৰ পুংখানুপুংখ সমাধান অন্তৰ্ভুক্ত কৰা হৈছে। অস্পীন একেডেমী (Ospin Academy) ত এই সমাধানসমূহ সহজ, নিৰ্ভুল আৰু সম্পূৰ্ণ পৰীক্ষামুখীভাৱে উপলব্ধ কৰোৱা হৈছে।
‘ৰাসায়নিক বিক্ৰিয়া আৰু সমীকৰণ’ নামৰ এই পাঠটিত আমাৰ দৈনন্দিন জীৱনত ঘটা ৰাসায়নিক পৰিৱৰ্তন, ৰাসায়নিক সমীকৰণ লিখা আৰু সমতুল কৰাৰ নিয়ম, লগতে বিভিন্ন প্ৰকাৰৰ ৰাসায়নিক বিক্ৰিয়া (যেনে- সংযোজন, বিয়োজন, অপসাৰণ, দ্বি-অপসাৰণ, জাৰণ আৰু বিজাৰণ) আদি সুন্দৰভাৱে বৰ্ণনা কৰা হৈছে। মেট্ৰিক পৰীক্ষাৰ্থীসকলৰ বাবে এই পাঠৰ মূল ধাৰণা বুজি পোৱাটো অতি প্ৰয়োজনীয়। আমাৰ এই পাঠ্যভিত্তিক সমাধানত (Textual Solutions) কেৱল পাঠ্যপুথিৰ অনুশীলনীৰ প্ৰশ্নসমূহেই নহয়, বৰঞ্চ পৰীক্ষাত আহিব পৰা অতিৰিক্ত গুৰুত্বপূৰ্ণ প্ৰশ্ন-উত্তৰসমূহো সামৰি লোৱা হৈছে যাতে ছাত্ৰ-ছাত্ৰীসকলে সুন্দৰভাৱে বিজ্ঞান বিষয়ৰ প্ৰস্তুতি চলাব পাৰে।
এই পাঠ্যভিত্তিক সমাধানৰ পৰা আপুনি কি কি শিকিব আৰু পাব:
- ৰাসায়নিক বিক্ৰিয়া আৰু সমীকৰণৰ মূল ধাৰণা আৰু বিস্তৃত পৰিচয়।
- সমতুলিত ৰাসায়নিক সমীকৰণ কেনেকৈ কৰিব লাগে তাৰ সহজ নিয়ম আৰু সমাধান।
- ১ নম্বৰৰ অতি চমু (VSA objective type), ২-৩ নম্বৰৰ চমু প্ৰশ্ন আৰু ৰাসায়নিক বিক্ৰিয়াৰ ওপৰত ভিত্তি কৰি দীঘলীয়া প্ৰশ্নৰ সহজ তথা মান্য সমাধান।
- বিক্ৰিয়াৰ প্ৰকাৰসমূহৰ (সংযোজন, বিয়োজন, অপসাৰণ আদি) প্ৰকৃত উদাহৰণসহ নিখুঁত উত্তৰ।
- নতুন পাঠ্যক্ৰমৰ আৰ্হি অনুসৰি গুৰুত্বপূৰ্ণ প্ৰশ্নসমূহৰ লগতে শেহতীয়া আৰ্হিৰ MCQ প্ৰশ্নৰ সমাধান।
অস্পীন একেডেমীৰ এই প্ৰশ্নোত্তৰসমূহৰ বিশেষ সুবিধা:
- শেহতীয়া ASSEB নতুন পাঠ্যক্ৰমৰ আধাৰত প্ৰস্তুত কৰা সম্পূৰ্ণ পাঠ্যভিত্তিক বিজ্ঞানৰ সমাধান।
- ১০০% নিৰ্ভুল আৰু ছাত্ৰ-ছাত্ৰীয়ে মুখস্থ কৰিবলৈ সহজ হোৱাকৈ সৰল অসমীয়া ভাষাত লিখা উন্নত মানৰ নোটছ (Class 10 Science Notes)।
- পৰীক্ষাৰ পূৰ্বে দ্ৰুত ৰিভিজনৰ (Quick Revision) বাবে বিশেষভাৱে যুগুতোৱা সহজ-সৰল উত্তৰ।
- বৰ্ণনামূলক প্ৰশ্নৰ লগতে পৰীক্ষাত আহিব পৰা অতিৰিক্ত গুৰুত্বপূৰ্ণ প্ৰশ্নৰ বিশেষ সংকলন।
ছাত্ৰ-ছাত্ৰীসকলৰ শৈক্ষিক উত্তৰণৰ প্ৰতি লক্ষ্য ৰাখি অস্পীন একেডেমীয়ে এই বিশেষ পাঠ্যভিত্তিক সমাধান আগবঢ়াইছে। আপোনাৰ মেট্ৰিক পৰীক্ষাৰ প্ৰস্তুতি এতিয়াই আৰম্ভ কৰক আৰু বিজ্ঞান বিষয়ত সৰ্বোচ্চ নম্বৰ লাভ কৰাৰ দিশত আগবাঢ়ক।
Class 10 Science (বিজ্ঞান) PDF Solutions 2026-27 | SEBA Assam
Download Class 10 Science (বিজ্ঞান) PDF with MCQs, textbook solutions, and additional practice questions for SEBA Assam 2025-26.
Textbook – Page 6
প্ৰ শ্না ৱ লী
1. বায়ুত দহনৰ আগতে মেগনেছিযামৰ ফিটা এডাল পৰিস্কাৰ কৰি ল’ব লাগে কিয় ?
উত্তৰ: মেগনেছিয়ামৰ ফিটা এডালৰ ওপৰত মেগনেচিয়াম অক্সাইড (MgO) ৰ তৰফ থাকে যিয়ে পুনৰ অক্সিজেনৰ লগত বিক্ৰিয়া কৰাত বাধা দিয়ে । সেয়েহে বায়ুত দহনৰ আগতে মেগনেছিয়ামৰ ফিটা এডাল পৰিস্কাৰ কৰি ল’ব লাগে।
2. তলৰ ৰাসায়নিক বিক্ৰিয়াবোৰৰ বাবে সন্তুলিত সমীকৰণ লিখা ।
(i) হাইড্ৰ’জেন + ক্ল’ৰিন → হাইড্ৰজেন ক্লৰাইড
(ii) বেৰিয়াম ক্ল’ৰাইড + এলুমিনিয়াম ছালফেট → বেৰিয়াম ছালফেট + এলুমিনিয়াম ক্ল’ৰাইড
(iii) ছ’ডিয়াম + পানী → ছ’ডিয়াম হাইড্ৰ’ক্সাইড +হাইড্ৰ’জেন
উত্তৰ : (i) H2 + Cl2 → 2HCl
(ii) 3BaCl2 + Al2(SO4)3 → 3BaSO4 + 2AlCl3
(iii) 2Na + 2H2O → 2NaOH + H2
3. তলৰ বিক্ৰিয়াবোৰৰ বাবে অৱস্থা চিহ্ন ( State Symbols) সহ একোটা সন্তুলিত ৰাসায়নিক সমীকৰণ লিখা ।
(i) বেৰিয়াম ক্ল’ৰাইড আৰু ছ’ডিয়াম ছালফেটৰ জলীয় দ্ৰৱৰ মাজত বিক্ৰিয়া ঘটি অদ্ৰাৱ্য বেৰিয়াম ছালফেট আৰু ছ’ডিয়াম ক্ল’ৰাইডৰ দ্ৰৱ প্ৰস্তত হয় ।
(ii) ছ’ডিয়াম হাইড্ৰ’ক্সাইড দ্ৰৱ (পানীত) হাইড্ৰ’ক্ল’ৰিক এছিডৰ (পানীত)ৰে সৈতে বিক্ৰিয়া কৰি ছ’ডিয়াম ক্ল’ৰাইডৰ দ্ৰৱ আৰু পানী উৎপন্ন কৰে ।
উত্তৰ:
(i) BaCl2 + (aq) + Na2SO4 → BaSO4 (S) + 2NaCl (aq)
(ii) 2NaOH (aq) +2HCl (aq) →2NaCl (aq) + H2O (l)
Textbook – Page no 10
1. এটা পদাৰ্থ ‘X’ দ্ৰৱক বগা ৰঙ সানিবলৈ (White washing) ব্যৱহাৰ কৰা হয় ।
(i) পদাৰ্থ ‘X’ ৰ নাম আৰু সংকেত লিখা ।
(ii) পানীৰে সৈতে পদাৰ্থ ‘X’ এ কৰা বিক্ৰিয়াটো লিখা ।
উত্তৰ: (i) পদাৰ্থ ‘X’ ৰ নাম : কেলছিয়াম অক্সাইড
সংকেত : CaO
(ii) পানীৰে সৈতে পদাৰ্থ ‘X’ এ কৰা বিক্ৰিয়াটো হ’ল –

2. কাৰ্যকলাপ 1.7 ত এটা পৰীক্ষানলত , সংগ্ৰহ কৰা গেছৰ পৰিমানণ আনটো পৰীক্ষানলত সংগ্ৰহ কৰা পৰিমানণ দূগুণ কিয় ? এই গেছটোৰ নাম লিখা ।
উত্তৰ :

ইয়াত ,
উৎপন্ন হোৱা হাইড্ৰ’জেন গেছৰ আয়তন অক্সিজেন গেছৰ দূগুণ । সেইবাবে এটা পৰীক্ষানলীত সংগ্ৰহ কৰা গেছৰ পৰিমাণ আনটো পৰীক্ষানলত সংগ্ৰহ কৰা পৰিমানণ দূগুণ ।
গেছটোৰ নাম : অক্সিজেন আৰু হাইড্ৰ’জেন ।
Textbook – Page no 13
1.লোৰ গজাল এটা ডুবাই ৰাখিলে ক’পাৰ ছালফেটৰ দ্ৰৱ এটাৰ ৰঙৰ পৰিৱৰ্বতন ঘটে কিয় ?
উত্তৰ: লো কপাৰতকৈ অধিক সক্ৰিয় গতিকে লোৱে ক’পাৰ ছালফেট দ্ৰৱ ক’পাৰ মৌলটোক অপসাৰিত কৰি আইৰণ ছালফেট উৎপন্ন কৰিছে । সেইবাবে দ্ৰৱটোৰ ৰঙৰ পৰিৱৰ্তন কৰিছে ।
এই বিক্ৰিয়াটোৰ ৰাসায়নিক হ’ব –
Fe (S) + CuSo4 (aq) → FeSo4 (aq) + Cu (S)
2. কাৰ্যকলাপ 1.10 ত দিয়া বিক্ৰিয়াটোৰ বাহিৰে আন এটা দ্বিঅপসৰন বিক্ৰিয়াৰ উদাহৰণ দিয়া ।
উত্তৰ: 2Cu + O2 → 2CuO
3. তলৰ বিক্ৰিয়া কেইটাত জাৰিত আৰু বিজাৰিত হোৱা পদাৰ্থসমূহ বাচি উলিওৱা
(i) 4Na (S) + O2 (g) → 2Na2 O(S)
(ii) CuO (S) + H2 (g) → Cu (S) + H2O (l)
উত্তৰ:
(i) 4Na (S) + O2 (g) → 2Na2O(S) → Na জাৰিত হৈ Na2O উৎপন্ন হৈছে ।
(ii) CuO (S) + H2 (g) →Cu (S)+ H2O(l) → CuO(S) বিজাৰণ হৈ Cu উৎপন্ন হৈছে আৰু H2 জাৰণ হৈ H2O উৎপন্ন হৈছে ।
(অনুশীলনী)
1. তলৰ বিক্ৰিয়াটোৰ বাবে উক্তিসমূহৰ কোনকেইটা অশুদ্ধ ?
2PbO (S) + C (S) → 2Pb (S) + CO2 (g)
(a) লেড বিজাৰিত হৈছে ।
(b) কাৰ্বন ডাই অক্সাইড জাৰিত হৈছে ।
(c) কাৰ্বন জাৰিত হৈছে ।
(d) লেড অক্সাইড বিজাৰিত হৈছে ।
(i) (a) আৰু (b)
(ii) (a) আৰু (c)
(iii) (a) , (b) আৰু (c)
(iv) সকলো
উত্তৰ: (i) (a) আৰু (b)
2. Fe2O3 + 2Al → Al2O3 + 2Fe
ওপৰতৰ বিক্ৰিয়াটো এটা উদাহৰণ
(a) এটা সংযোজন বিক্ৰিয়াৰ
(b) এটা দ্বিঅপসৰণ বিক্ৰিয়াৰ
(c) এটা বিযোজন বিক্ৰিয়াৰ
(d) এটা অপসৰণ বিক্ৰিয়াৰ
উত্তৰ: (d) এটা অপসৰণ বিক্ৰিয়াৰ
3. কি ঘটে যেতিয়া লঘু হাইড্ৰ’ক্লৰিক এছিড লোৰ গুৰিত যোগ কৰা হয় ? শুদ্ধ উত্তৰটো টিক চিন দিয়া ।
(a) হাইড্ৰজেন গেছ আৰু আইৰণ ক্ল’ৰাইড উৎপন্ন হয় ।
(b) ক্ল’ৰিন গেছ আৰু আইৰণ হাইড্ৰ’ক্সাইড উৎপন্ন হয় ।
(c) বিক্ৰিয়া নঘটে ।
(d) আইৰণ লৱণ আৰু পানী উৎপন্ন হয় ।
উত্তৰ: (a) হাইড্ৰজেন গেছ আৰু আইৰণ ক্ল’ৰাইড উৎপন্ন হয় ।
4. সন্তুলিত ৰাসায়নিক সমীকৰণ কি ? ৰাসায়নিক সমীকৰণসমূহ কিয় সন্তুলিত কৰিব লাগে ?
উত্তৰ: সন্তুলিত ৰাসায়নিক সমীকৰণ হৈছে এনে এটা ৰাসায়নিক সমীকৰণ য’ত বিক্ৰিয়ক আৰু বিক্ৰিয়জাত পদাৰ্থৰ প্ৰতিটো উপাদান মৌলৰ সমান সংখ্যক পৰমানু থাকে ।
ভৰৰ নিত্যতা বিধি অনুসৰি “ৰাসায়নিক বিক্ৰিয়া এটাত ভৰৰ সৃষ্টি বা নাশ হ’ব নোৱাৰে । সেয়েহে ভৰৰ নিত্যতা বিধি অনুসৰি ৰাসায়নিক সমীকৰণ সন্তুলিত হোৱাৰ প্ৰয়োজন ।
5. তলৰ উক্তিসমূহৰ ৰাসায়নিক সমীকৰণৰ ৰূপত লিখা আৰু সন্তুলন কৰা ।
(a) হাইড্ৰ’জেন গেছে নাইট্ৰ’জেনেৰে সৈতে লগ হৈ এম’নিয়া প্ৰস্তত কৰে ।
উত্তৰ: H2 + N2 → NH3
সমতুল ৰাসায়নিক সমীকৰণ
3H2 (g) + N2 → 2NH3 (g)
(b) হাইড্ৰ’জেন ছালফাইডে বায়ুত দাহিত হৈ পানী আৰু ছালফাৰ ডাই অক্সাইড উৎপন্ন কৰে।
উত্তৰ: H2S + O2 → H2O + SO2
সমতুল ৰাসায়নিক সমীকৰণ
2H2S (g) + 3O2 → 2H2O (l) + 2SO2 (g)
(c) বেৰিয়াম ক্ল’ৰাইডে এলুমিয়াম ছালফেটেৰে সৈতে বিক্ৰিয়া কৰি এলুমিয়াম ক্ল’ৰাইড আৰু বেৰিয়াম ছালফেটৰ অধ:ক্ষেপ উৎপন্ন কৰে ।
উত্তৰ: BaCl2 + Al2(SO4)3 → BaSO4 + AlCl3
সমতুল ৰাসায়নিক সমীকৰণ
3BaCl2 (aq) + Al2(SO4)3 (aq) → 3BaSO4 (s) + 2AlCl3 (aq)
(d) পটেছিয়াম ধাতুয়ে পানীৰে সৈতে বিক্ৰিয়া কৰি পটেছিয়াম হাইড্ৰ’ক্সাইড আৰু হাইড্ৰ’জেন গেছে উৎপন্ন কৰে ।
উত্তৰ: K + H2O → KOH + H2
সমতুল ৰাসায়নিক সমীকৰণ
2K (s) + 2H2O → 2KOH (aq) + H2 (g)
6. তলৰ ৰাসায়নিক সমীকৰণসমূহ সন্তুলন কৰা ।
(a) HNO3 + Ca (OH)2 → Ca (NO3)2 + H2 O
উত্তৰ: 2HNO3 + Ca (OH)2 → Ca (NO3)2 + 2H2O
(a) NaOH + H2SO4 → Na2SO4 + H2O
উত্তৰ: 2NaOH + H2SO4 → Na2SO4 + H2O
(c) NaCl + AgNO3 → AgCl + NaNO3
উত্তৰ: NaCl + AgNO3 → AgCl + NaNO3
(d) BaCl2 + H2SO4 → BaSO4 + HCl
উত্তৰ: BaCl2 + H2SO4 → BaSO4 + 2HCl
7. তলৰ বিক্ৰিয়াবোৰৰ বাবে সন্তুলিত ৰাসায়নিক সমীকৰণবোৰ লিখা ।
(a) কেলছিয়াম হাইড্ৰ’ক্সাইড + কাৰ্বন ডাই অক্সাইড → কেলছিয়াম কাৰ্বনেট + পানী ।
উত্তৰ: Ca(OH)2 (aq) + CO2 (g) → CaCO3 (aq) + H2O (l)
(b) যিংক + ছিলভাৰ নাইট্ৰেট → যিংক নাইট্ৰেট + ছিলভাৰ ।
উত্তৰ: Zn (s) + 2AgNO3 (aq) → Zn(NO3)2 (aq) + 2Ag (s)
(c) এলুমিনিয়াম + ক’পাৰ ক্ল’ৰাইড → এলুমিনিয়াম ক্ল’ৰাইড + ক’পাৰ ।
উত্তৰ: 2Al (s) + 3CuCl2 (aq) → 2AlCl3 (aq) + 3Cu (s)
(d) বেৰিয়াম ক্ল’ৰাইড + পটেছিয়াম ছালফেট → বেৰিয়াম ছালফেট + পটেছিয়াম ক্ল’ৰাইড ।
উত্তৰ: BaCl2 (s) + K2SO4 (aq) → BaSO4 (aq) + 2KCl (s)
8. তলত দিয়াবোৰৰ বাবে সন্তুলিত ৰাসায়নিক সমীকৰণ লিখা আৰু প্ৰতিটো কোন প্ৰকাৰৰ বিক্ৰিয়া চিনাক্ত কৰা ।
(a) পটেছিয়াম ব্ৰ’মাইড (aq) + বেৰিয়াম আয়’ডাইড (aq) → পটেছিয়াম আয়’ডাইড (aq) + বেৰিয়াম ব্ৰ’মাইড (S)
(c) যিংক কাৰ্বনেট (S) → যিংক অক্সাইড (S) + কাৰ্বন ডাই অক্সাইড (g)
(c) হাইড্ৰ’জেন (g) + ক্ল’ৰিন (g) → হাইড্ৰ’জেন ক্ল’ৰাইড (g)
(d) মেগনেছিয়াম (s) + হাইড্ৰ’ক্ল’ৰিক এছিড (aq) → মেগনেছিয়াম ক্ল’ৰাইড (aq) + হাইড্ৰ’জেন (g)
উত্তৰ:
|
ক্ৰমিক নং |
সমতুল ৰাসায়নিক সমীকৰণ |
বিক্ৰিয়াৰ প্ৰকাৰ |
|---|---|---|
|
(a) |
2KBr (aq) + BaI2 (aq) → 2KI (aq) + BaBr2 (s) |
দ্বিঅপসৰণ বিক্ৰিয়া |
|
(b) |
ZnCO3 (s) → ZnO (s) + CO2 (g) |
বিযোজন বিক্ৰিয়া |
|
(c) |
H2 (g) + Cl2 (g) → 2HCl (g) |
সংযোজন বিক্ৰিয়া |
|
(d) |
Mg (s) + 2HCl (aq) → MgCl2 (aq) + H2 (g) |
অপসৰণ বিক্ৰিয়া |
9. তাপবৰ্জী আৰু তাপগ্ৰাহী বিক্ৰিয়া বুলিলে কি বুজা ? উদাহৰণ দিয়া ।
উত্তৰ: যি ৰাসায়নিক বিক্ৰিয়াত বিক্ৰিয়াজাত পদাৰ্থ উৎপন্ন হোৱাৰ লগতে তাপৰ উদ্ভৱ হয় তাকে তাপবৰ্জী বিক্ৰিয়া বোলে ।
উদাহৰণস্বৰূপে: মিথেন গেছে বায়ুত অক্সিজেনৰ উপস্থিতিত জ্বলি কাৰ্বন ডাই অক্সাইড আৰু পানী উৎপন্ন কৰাৰ লগতে যথেষ্ট পৰিমাণৰ তাপ শক্তি উৎপন্ন কৰে ।
CH4 (g) + 2O2 (g) → CO2 (g) + 2H2O (g) + তাপ শক্তি
আনহাতে ,
যি ৰাসায়নিক বিক্ৰিয়াত শক্তি বা তাপ শোষিত হয় তাকে তাপগ্ৰাহী বিক্ৰিয়া বোলে ।
উদাহৰণস্বৰূপে: ছিলভাৰ ক্ল’ৰাইড আৰু ক্ল’ৰিন সূৰ্যৰ পোহৰৰ উপস্থিতিত ছিলভাৰ উৎপন্ন কৰাৰ লগতে ক্ল’ৰিন উৎপন্ন কৰে ।

10. শ্বসনক এটা তাপবৰ্জী বিক্ৰিয়া বুলি কিয় বিবেচনা কৰা হয় ? বাখ্যা কৰা ।
উত্তৰ: শ্বসন এনে এটা প্ৰক্ৰিয়া য’ত জৈৱিক পদাৰ্থসমূহৰ বিভংগন ঘটি শক্তি মুক্ত হোৱাৰ লগতে সৰল বিক্ৰিয়াজাত পদাৰ্থ উৎপন্ন হয় । যাক পৰৱৰ্তী পৰ্যায়ত দেহৰ বিভিন্ন ক্ৰিয়াকলাপত ব্যৱহাৰ কৰা হয় । পাচন প্ৰক্ৰিয়াত খাদ্যত থকা কাৰ্ব’হাইড্ৰেট গ্লক’জলৈ বিযোজিত হয় । এই গ্লক’জে দেহৰ কোষত অক্সিজেনৰ সৈতে বিকেৰিয়া কৰি কাৰ্বন ডাই অক্সাইড আৰু পানী উৎপন্ন কৰাৰ লগতে শক্তি উৎপন্ন কৰে ।
বিক্ৰিয়াটোৰ ৰাসায়নিক সমীকৰণ হৈছে :-
C6H12O6 (aq) + 6O2 (aq) → 6CO2 (g) + 6H2O (l) + শক্তি
এই বিক্ৰিয়াত শক্তি উতপন্ন হোৱা বাবে ইয়াক তাপবৰ্জী বিক্ৰিয়া হিচাপে বিবেচনা কৰা হয় ।
11. বিযোজন বিক্ৰিয়াক সংযোজন বিক্ৰিয়াৰ বিপৰীত বোলা হয় কিয় ? এই সমূহ বিক্ৰিয়াৰ বাবে সমীকৰণ লিখা ।
উত্তৰ: সংযোজন বিক্ৰিয়াত দুটা বা ততোধিক পদাৰ্থ (মৌল যৌগ) যোজিত হৈ নতুন পদাৰ্থ উৎপন্ন কৰে ।
উদাহৰণস্বৰূপে: অক্সিজেনৰ উপস্থিতিত হাইড্ৰ’জেনক দাহিত কৰিলে ই এক শিখা জ্বলি পানী উৎপন্ন কৰে ।
2H2 (g) + O2 (g) → 2H2 (g)
বিযোজন বিক্ৰিয়াত এটা ৰাসায়নিক পদাৰ্থ বা যৌগ বিযোজিত হৈ দুটা ততোধিক পদাৰ্থ উৎপন্ন হয় ।
উদাহৰণস্বৰূপে: পানীত বিদ্যুত বিশ্লেষণ কৰিলে হাইড্ৰ’জেন গেছ আৰু অক্সিজেন গেছ উৎপন্ন হয় ।

12 . তাপ , পোহৰ আৰু বিদ্যুৎ শক্তিৰে সংঘটিত বিযোজন বিক্ৰিয়াৰ একোটাকৈ সমীকৰণ লিখা ।
উত্তৰ :

13. অপসৰণ আৰু দ্বিঅপসৰণ বিক্ৰিয়াৰ মাজত পাৰ্থক্য কি ? এই বিক্ৰিয়াটোৰ বাবে সমীকৰণ লিখা ।
উত্তৰ: এবিধ ৰাসায়নিক বিক্ৰিয়া য’ত অধিক সক্ৰিয় মৌল এটাই কম সক্ৰিয় মৌল এটাক ইয়াৰ যৌগ দ্ৰৱৰ পৰা অপসাৰিত কৰে তেনে ৰাসায়নিক বিক্ৰিয়াক অপসৰণ বিক্ৰিয়া বোলে ।
যেনে : সমীকৰণ অপসৰণ বিক্ৰিয়াৰ :
Mg (s) + 2HCl (aq) → MgCl2 (aq) + H2 (g)
এবিধ ৰাসায়নিক বিক্ৰিয়া য’ত দুটা বিক্ৰিয়কে আয়ন বিনিময় কৰি নতুন বিক্ৰিয়াজাত পদাৰ্থ উতপন্ন হয় তেনে ৰাসায়নিক বিক্ৰিয়াক দ্বিঅপসৰণ বিক্ৰিয়াৰ বোলে ।
যেনে: সমীকৰণ অপসৰণ বিক্ৰিয়াৰ :
2KBr (aq) + BaI2 (aq) → 2KI (aq) + BaBr2 (s)
14. ছিলভাৰ সংশোধনত ছিলভাৰ নাইট্ৰেট দ্ৰৱ পৰা আহৰণ কৰোঁতে ক’পাৰ ধাতুৰদ্বাৰা অপসাৰণ সংঘটিত কৰা হয় । জড়িত বিক্ৰিয়াটো লিখা ।
উত্তৰ: AgNO3 (aq) + Cu (s) → Cu (NO3)2 (aq) + 2Ag (s)
15. অধ:ক্ষেপণ বিক্ৰিয়া মানে কি বুজা ? উদাহৰণ দি বাখ্যা কৰা ।
উত্তৰ: যি বিক্ৰিয়াৰই অধ:ক্ষেপ উৎপন্ন কৰে (পানীত অদ্ৰৱণীয় গোটা পদাৰ্থ) তাকে অধ:ক্ষেপণ বিক্ৰিয়া বোলে ।
উদাহৰণ: ক’পাৰ ছালফেটৰজলীয় দ্ৰৱৰ মাজেৰে হাইড্ৰ’জেন ছালফাইড গেছ যাব দিলে কপাৰ ছালফাইডৰ এটা ক’লা অধ:ক্ষেপ আৰু ছ’ডিয়াম নাইট্ৰেট দ্ৰৱ উৎপন্ন হয় ।
CuSO4 (aq) + H2S (g) → CuS (s) + H2SO4 (aq)
16. অক্সিজেন লাভ আৰু হেৰুৱা সংজ্ঞাৰে তলৰ পদসমূহ বাখ্যা কৰা ।
(a) জাৰণ ।
(b) বিজাৰণ ।
উত্তৰ: (a) জাৰণ :- যি বিক্ৰিয়াত কোনো এটা পদাৰ্থৰ লগত অক্সিজেন যোগ হয় তাকে জাৰণ বিক্ৰিয়া বোলে ।
উদাহৰণস্বৰূপে: S (s) + O2 (g) → SO2 (g)
ছালফাৰে অক্সিজেন লাভ কৰি ছালফাৰ ডাই অক্সাইড উৎপন্ন কৰে ।
(b) বিজাৰণ :- যি বিক্ৰিয়াত কোনো এটা পদাৰ্থই অক্সিজেন হেৰুৱাই তাকে জাৰণ বিক্ৰিয়া বোলে ।
ZnO (s) + C (g) → Zn (s) + CO (g)
যিংক অক্সাইড ৰ পৰা অক্সিজেন অপসাৰিত হৈছে ।
17. এটা উজ্জল মুগা ৰঙৰ মৌল ‘X’ ক বায়ুত গৰম কৰাত ক’লা হৈ পৰিল । মৌল ‘X’ আৰু উৎপন্ন হোৱা ক’লা ৰঙৰ যৌগটোৰ নাম লিখা ।
উত্তৰ : উজ্জল মুগা ৰঙৰ মৌল ‘X’ হৈছে কপাৰ (Cu) আৰু উৎপন্ন হোৱা ক’লা ৰঙৰ যৌগটো হৈছে ক’পাৰ (II) অক্সাইড (CuO
তলত দিয়া ৰাসায়নিক বিক্ৰিয়াটো সংঘটিত হৈছে :
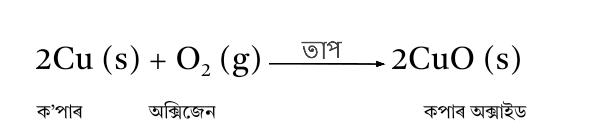
18. লোৰ বস্তুত ৰঙৰ প্ৰলেপ দিও কিয় ?
উত্তৰ: নিয়মীয়া সময়ৰ ব্যৱধানত লোৰ সামগ্ৰীৰ পৃষ্ঠভাগত ৰং প্ৰয়োগৰে মামৰ প্ৰতিৰোধ কৰিব পৰি । লোৰ বস্তুবোৰ বায়ুৰ জলীয় বাষ্পৰ সংস্পৰ্শত লো ফেৰাছ অক্সাইডলৈ জাৰিত হয় যি সংশ্লিষ্ট বস্তুৰ ওপৰত মামৰ বুলি কোবা ৰঙচুৱা মুগা বৰণৰ তৰপ হিচাপে বিৰাজ কৰে । সামগ্ৰীৰ পৃষ্ঠভাগত ৰঙে এক সুৰক্ষা প্রদায়ক প্রলেপ গঠন আ্রৰু এই প্রলেপে ধাতবীয় পৃষ্ঠৰ সৈতে বায়ুৰ আর্দ্রতাৰ সংস্পৰ্শত প্রতিৰোধ কৰি মামৰ সৃষ্টি হোবাত বাধা দিয়ে ।
19. তেল আৰু চৰ্বি থকা খাদ্যবস্তু নাইট্ৰ’জেনৰ পৰিৱেশত পেকেটত ভৰোৱা হয় কিয় ?
উত্তৰ: তেল আৰু চৰ্বি থকা খাদ্যবস্তু নাইট্ৰ’জেনৰ পৰিৱেশত পেকেটত ভৰোৱা হয় কিয়নো নাইট্র’জেনে প্রতিজাৰক হিচাপে কাম কৰে যাৰ ফলত বায়ুৰ অক্সিজেনৰ পৰিৱেশত জাৰণ ঘটিব নোবাৰে । এনেদৰে দুর্গন্ধিতা বা ৰেনচিডিটি প্রতিৰোধ কৰিব পাৰি ।
20. এটা উদাহৰণৰে সৈতে তলৰ পদসমূহ বাখ্যা কৰা ।
(a) ক্ষয়ীভৱন ।
(b) চৰ্বিৰ দুৰ্গন্ধিতা ।
উত্তৰ:
(a) ক্ষয়ীভৱন :- জলীয় বাষ্প , এছিড আদিৰ প্রভাবত ধাতুৰ পৃষ্ঠভাগর অবক্ষয় সাধন হোবা প্রক্রিয়াটোয়েই হৈছে ক্ষয়ীভৱন । ক্ষয়ীভৱন প্রক্রিয়াই ধাতুৰে তৈয়াৰী সকলোবোৰ বস্তু বিশেষকৈ লোৰে তৈয়াৰী বস্তু যেনে – গাড়ী-মটৰ , দলং , জাহাজ আদিৰ ক্ষতিসাধন কৰি জটিল সমস্যাৰ সৃষ্টি কৰে ।
বিভিন্ন ধাতুৰ ওপৰত ক্ষয়ীভৱনৰ কেইটামান প্ৰভাৱ হৈছে :
(i) লোৰ ওপৰত ৰঙচুৱা মুগা বৰণৰ পাউদাৰৰ চামনি পৰে ।
(ii) ছিলভাৰৰ ওপৰত ক’লা চামনি পৰে ।
(iii) কপাৰৰ ওপৰত সেউজীয়া চামনি পৰে ।
উদাহৰণ : লোত মামৰে ধৰাটো সচৰাচৰ পৰিলক্ষিত হোৱা এবিধ ক্ষয়ীভৱন । লোৰ সামগ্ৰীবোৰত বায়ুৰ আৰ্দ্ৰতাৰ সংস্পৰ্শত ৰঙচুৱা মুগা বৰণৰ চামনি পৰে ।
(b) চৰ্বিৰ দুৰ্গন্ধিতা :- তেল অথবা চৰ্বিযুক্ত খাদ্য দীৰ্ঘসময়ৰ কাৰণে ৰাখি থলে বেয়া গোন্ধ তথা বেয়া স্বাদৰ সৃষ্টি হয় । ইয়াৰ কাৰণে এয়েই যে এনে খাদ্য দ্ৰব্যত থকা তেল আৰু চৰ্বি বায়ুৰ অক্সিজেনৰ দ্বাৰা জাৰিত হয় । এই পৰিঘটনাক দুৰ্গন্ধিতা বা ৰেনচিডিটি বুলি কোৱা হয় ।
দুৰ্গন্ধিতা প্ৰতিৰোধ বা মন্থৰ কৰাৰ পদ্ধতিসমূহ :
(i) চৰ্বিযুক্ত বা তেলযুক্ত খাদ্যসমূহত প্ৰতিজাৰক (জাৰণ প্ৰতিৰোধ কৰা দ্ৰৱ্য) যোগ কৰি দুৰ্গন্ধিতা প্ৰতিৰোধ কৰিব পাৰি ।
(ii) বায়ুৰোধী পাত্ৰত ৰখা খাদ্যই জাৰণ প্ৰতিৰোধ কৰে ।
(iii) চৰ্বিযুক্ত বা তেলযুক্ত খাদ্যসমূহত নাইট্ৰ’জেন যোগ কৰা হয় যাতে সেইবোৰ জাৰিত নহয় ।
উদাহৰণ : গ্ৰীষ্মকালত মুকলি ঠাইত ৰখা মাখনত কিছুদিনৰ পাছত গোন্ধ আৰু স্বাদ সলনি হয় ।


Sir important diok